近日,我院分子病毒學研究團隊孫麗英教授課題組在《Advanced Science》上發(fā)表了題為“A Viral RNA Silencing Suppressor Modulates Reactive Oxygen Species Levels to Induce the Autophagic Degradation of Dicer-like and Argonaute-like Proteins”的研究論文。該研究綜合運用分子生物學、遺傳轉(zhuǎn)化及生理生化等一系列研究手段,發(fā)現(xiàn)板栗疫病菌低毒病毒1(CHV1)在其宿主真菌中采用了一種新穎且復雜的反防御策略。該機制通過病毒編碼的沉默抑制子p29蛋白抑制宿主真菌中的FMN還原酶,進而調(diào)控細胞內(nèi)活性氧(ROS)水平。這一改變誘發(fā)了宿主抗病毒關鍵組分DCL2(Dicer-like)和AGL1(Argonaute-like)蛋白的自噬降解,最終降低了宿主的抗病毒RNAi應答能力。
在病毒感染過程中,病毒需要應對宿主多種抗病毒防御機制的抑制,這些機制旨在限制其復制、傳播及致病性。因此,病毒必須主動調(diào)控宿主的生理狀態(tài)以突破此類限制。越來越多的證據(jù)表明,病毒感染會引發(fā)宿主細胞內(nèi)氧化還原穩(wěn)態(tài)失衡,導致活性氧(ROS)水平上升,而病毒可利用這一變化促進自身復制與感染進程。然而,關于病毒如何精確利用ROS信號以增強感染的分子機制,目前仍知之甚少。
CHV1是研究最為深入的真菌病毒之一,能夠顯著減弱板栗疫病菌( Cryphonectria parasitica )的致病性,被認為是一種潛力顯著的生物防治制劑,同時也是研究病毒與宿主互作的理想模型系統(tǒng)。該病毒所編碼的p29蛋白屬于木瓜蛋白酶樣蛋白酶,在病毒積累、存活、傳播以及癥狀表達等多個方面發(fā)揮關鍵作用,具有多樣的調(diào)控功能。已有研究表明,p29可通過抑制栗疫病菌中關鍵抗病毒RNA沉默基因 DCL2 和 AGL2 的轉(zhuǎn)錄上調(diào),從而有效抑制宿主的RNA沉默通路。盡管p29的多功能性已得到較多揭示,其發(fā)揮作用的分子機制仍不完全清楚。
為闡明CHV1 p29蛋白調(diào)控真菌生理過程的分子機制,本研究在禾谷鐮刀菌( Fusarium graminearum )中對p29的宿主互作蛋白進行了系統(tǒng)性篩選,發(fā)現(xiàn)黃素單核苷酸還原酶1(FMR1)與p29發(fā)生特異性相互作用。在CHV1感染后, FMR1 的轉(zhuǎn)錄水平顯著上升,且功能實驗表明該蛋白正調(diào)控宿主對CHV1的病毒抗性。進一步研究發(fā)現(xiàn),在CHV1感染過程中,p29與FMR1結合并抑制其活性,誘發(fā)宿主發(fā)生氧化應激,導致細胞內(nèi)活性氧(ROS)大量積累,從而促進了CHV1的病毒復制與穩(wěn)定性。病毒增殖與ROS水平之間形成正向反饋循環(huán),致使宿主細胞內(nèi)氧化還原穩(wěn)態(tài)失衡,最終激活自噬通路。自噬關鍵蛋白ATG8作為貨物受體,可與RNA沉默通路中的核心組分DCL2和AGL1結合,介導二者通過自噬途徑降解,從而顯著削弱宿主的核心抗病毒防御能力。該研究揭示了CHV1通過p29蛋白的多功能活性精密調(diào)控氧化應激、自噬與RNA沉默三者之間的互作網(wǎng)絡,為理解病毒通過協(xié)同操縱多種宿主防御系統(tǒng)以建立感染的分子機制提供了重要理論模型。
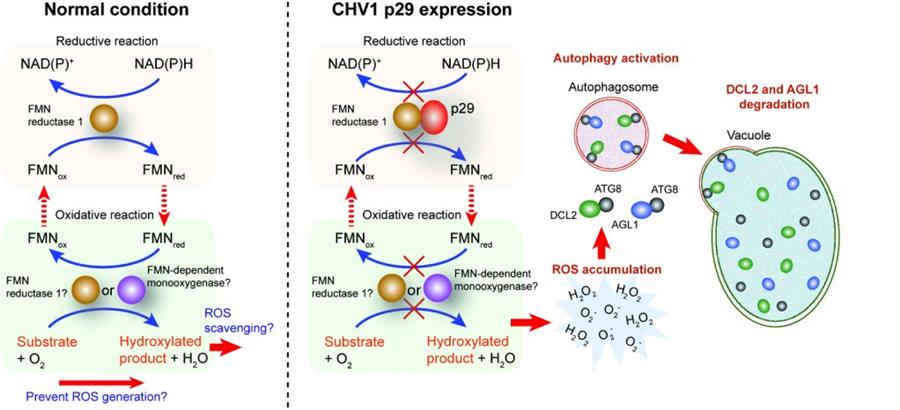
CHV1 p29通過抑制FMN還原酶活性誘導DCL2和AGL1自噬降解的模式圖
我院博士畢業(yè)生翟世玉為本文第一作者,孫麗英教授與Ida Bagus Andika教授為共同通訊作者。課題組在讀博士生龐天興和碩士生彭詩瑜參與了研究工作。本研究得到了康振生院士及日本岡山大學資源植物科學研究所鈴木信宏教授的指導,以及山東農(nóng)業(yè)大學植保學院鄒申申教授、浙江省農(nóng)業(yè)科學院病毒學研究所鄧志平研究員的重要技術支持。旱區(qū)作物脅迫生物學國家重點實驗室趙華博士與學院科技創(chuàng)新與人才培養(yǎng)平臺李艷為本研究提供了技術支持,我院劉慧泉教授和江聰教授提供了實驗材料支持。此外,德國馬克斯普朗克植物分子生理學研究所的Marion Clavel博士和Marco Incarbone博士在研究過程中參與了科學討論,為本工作提供了寶貴建議。該研究受到校雙一流項目、未來院前沿交叉團隊項目、國家自然科學基金項目的資助。
文章鏈接:https://doi.org/10.1002/advs.202506572
編輯:劉小鳳
審核:趙 磊

